La présence de cliniciens au sein du laboratoire, et plus généralement les interactions étroites de ses chercheurs avec leurs collègues cliniciens, nous amène à bien connaître les limites de ces dispositifs. Le laboratoire travaille en lien étroit avec le Centre d’Investigation Clinique – Innovation Technologique (CHU Grenoble Alpes), qui conçoit un « observatoire des dispositifs médicaux ». Les chercheurs ont proposé des innovations sur de nombreux dispositifs médicaux. Ainsi, un microscope original à bi-réfringence a été conçu pour analyser l’orientation des fibres du cœur, ouvrant la voie à un modèle inédit de sa morphogénèse. Des modèles biomécaniques capables de caractériser le risque de rupture d’une plaque athéromateuse ont pu être intégrés dans des échographes vasculaires. Un T-shirt connecté capable d’analyser le mouvement du torse du patient (destiné dans un premier temps à permettre de dépasser les limites des corsets proposés aux patients scoliotiques). Ces travaux se prolongent régulièrement et naturellement en actions de transfert ou de création de startups avec le support de la SATT grenobloise Linksium. Deux exemples caractéristiques de la conception de solutions permettant de dépasser les limites des dispositifs de suivi des pathologies cardio-vasculaire ont conduit récemment à la création des startups SentinHealth et Etisense. Il est intéressant de mettre en regard les approches et stratégies respectives choisies dans les deux cas. SentinHealth développe un dispositif implantée dans l’estomac et Etisense une solution non-invasive intégrée dans un vêtement intelligent. Les logiques peuvent apparaître en opposition mais elles relèvent en fait d’un même principe fondateur et fédérateur des actions d’innovation du laboratoire en matière de dispositifs : respecter la physiologie pour mieux l’observer et préserver le bien-être du sujet pour minimiser bruits et biais potentiels. Dans les deux cas on cherche à optimiser les conditions d’accès à l’information cardiaque ainsi que les conditions d’usage. Dans les deux cas on accède au site de mesure, que le capteur soit implanté ou non, par voies anatomiques externes.
Le Gilet intelligent d’Etisense
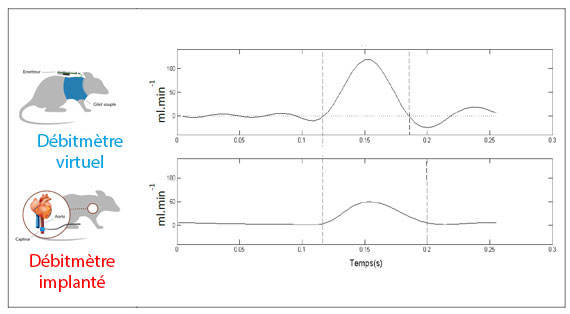
Il repose sur une technologie de « débitmétrie virtuelle » [1] qui permet une estimation de paramètres mécaniques cardiorespiratoires à l’aide d’une observation en périphérie du tronc. Le dispositif non-invasif mesure avec une résolution adaptée, les variations de volume du thorax induites par les activités respiratoires et cardiaques [2,3]. Cette technologie s’applique à l’humain comme au petit animal de laboratoire. On peut ainsi mesurer des variations de volumes qui vont de quelques litres (volume respiratoire humain) à quelques dizaines de microlitres (éjection cardiaque d’un petit rongeur de laboratoire).

Des modèles mathématiques et des traitements de signaux appropriés permettent de construire des profils de débit aortique sous-diaphragmatique dont la mesure n’est accessible que par l’intermédiaire d’un débitmètre placé autour de l’aorte par le biais d’une intervention chirurgicale.
Le stéthoscope numérique de SentinHealth
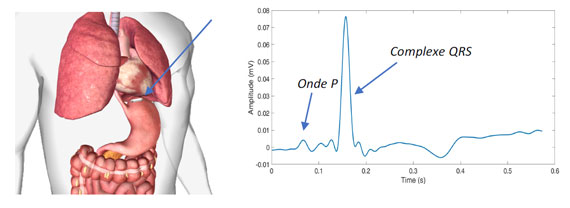
On choisit cette fois un site d’observation au plus proche du cœur. Un implant miniaturisé [4] est fixé à la muqueuse gastrique, à quelques millimètres seulement du cœur. Le stéthoscope numérique miniature permet alors une surveillance continue des paramètres cardiaques pour une détection précoce de la décompensation d’une insuffisance cardiaque. On parle ici de dispositif "sentinelle" pour lequel l’observance est optimale du fait du site d’implantation. Cette approche innovante est explorée en collaboration avec des cardiologues et des spécialistes d’endoscopie interventionnelle du CHUGA. Soulignons que l’accès au site d’implantation se fait de façon minimalement invasive par endoscopie. Le positionnement retenu permet de résoudre les problèmes de biocompatibilité.
Les deux dispositifs présentés sont en réalité multi-modaux et intègrent différents types de capteurs. Les traitements avancés des biosignaux prélevés permettent d’extraire un ensemble de paramètres physiologiques et de biomarqueurs dans des conditions de mesure ambulatoire. Ces valeurs alimentent alors des technologies d’Intelligence Artificielle. On construit ainsi des outils numériques d’aide au diagnostic clinique basés sur des modèles explicatifs cliniquement pertinents.
Références :
- [1] P. Baconnier, F. Boucher, P.Y. Gumery. Device and method for non-invasive measurement of subdiaphragmatic aortic flow in a small laboratory mammal. US2018279887 (A1) - 2018-10-04
- [2] J. Fontecave-Jallon, T. Flenet, C. Eynard, P.Y. Gumery, F. Boucher, S. Tanguy. Inductive plethysmography in rats : towards a new standard for longitudinal non-invasive cardiac output monitoring in preclinical studies. Physiological Measurement, IOP Publishing, 2018, 39 (9).
- [3] T. Flenet, J. Fontecave-Jallon, P.Y. Gumery, C. Eynard, F. Boucher, P. Baconnier, S. Tanguy. High-resolution respiratory inductive plethysmography in rats : validation in anesthetized conditions. Physiological Measurement, IOP Publishing, 2017, 38 (7), pp.1362 - 1372
- [4] P. Cinquin, F. Boucher, P. Defaye, P.Y. Gumery, P. Tuvignon. Implantable system. WO2018104472 (A1) - 2018-06-14
